O custo do tratamento do câncer de mama por paciente no SUS
Introdução O câncer de mama é a neoplasia mais incidente em mulheres, sendo um problema de saúde pública na maior parte do mundo[1]. As taxas ajustadas de incidência para o câncer de mama são as maiores tanto em países com alto IDH- Índice de Desenvolvimento Humano (55,9 por 100 mil) quanto naqueles considerados com baixo […]
Custo do câncer no SUS

INTRODUÇÃO O câncer, tanto no Brasil, como no mundo todo, representa um dos maiores desafios de saúde pública, desde a prevenção, diagnóstico, até o controle da doença. De acordo com estimativas feitas em 2019 pela Organização Mundial da Saúde (OMS), o câncer é a primeira ou segunda principal causa de morte antes dos 70 anos […]
Panorama do Mieloma Múltiplo no SUS

Introdução O mieloma múltiplo (MM) é uma forma maligna de câncer que se origina a partir da expansão descontrolada de plasmócitos malignos da medula óssea1,2 e representa 1% de todas as neoplasias malignas prevalentes globalmente e 10 a 15% dos cânceres hematológicos2,3,4. Segundo a Agência Internacional para Pesquisa em Câncer da Organização Mundial de Saúde […]
Impacto da pandemia de covid-19 em procedimentos com finalidade diagnóstica no sistema único de saúde (SUS)

Os coronavírus são uma ampla família de vírus que podem causar uma variedade de condições, do resfriado comum a doenças mais graves, como a síndrome respiratória do Oriente Médio (MERS-CoV) e a síndrome respiratória aguda grave (SARS-CoV). O novo coronavírus, denominado SARS-CoV-2, causador da doença COVID-19 foi detectado após a notificação de um surto em […]
Panorama da atenção de Leucemia Mieloide Aguda no SUS

INTRODUÇÃO Em 2020, foram estimados no mundo 475 mil casos de leucemia, o que equivale a 2,5% de todos os tipos de câncer. (FERLAY et al., 2020 apud INCA, 2023). Segundo o Instituto Nacional do Câncer (INCA), no Brasil para cada ano triênio de 2023 a 2025 são estimados cerca de 11.540 novos casos de […]
Panorama da atenção ao câncer de mama no SUS

O câncer de mama é a neoplasia mais comumente diagnosticada em mulheres, configurando-se em importante problema de saúde pública mundial devido à sua elevada incidência e morbimortalidade (Santos et al, 2022). No Brasil, segundo o Instituto Nacional do Câncer (INCA), estimam-se cerca de 74 mil casos novos de câncer de mama para o ano de […]
Câncer como a primeira causa de morte nos municípios brasileiros

O câncer é uma importante barreira para o aumento da expectativa de vida em todos os países do mundo (1). Segundo estimativas da Organização Mundial da Saúde (OMS), em 2019 o câncer é a primeira ou segunda causa principal de morte antes dos 70 anos em 112 dos 183 países (2). No Brasil, o câncer […]
Impacto da covid-19 na oncologia
Sem dúvidas, combater a pandemia e, ao mesmo tempo, manter a prestação de serviços de saúde de qualidade para controle e combate à outras condições e agravos à saúde é um grande desafio. Os sistemas de saúde em geral, assim como no Brasil, não estavam preparados para atender de forma rápida e coordenada as necessidades […]
Saúde da mulher: Prevenção do Câncer do Colo do Útero
O câncer do colo do útero, também chamado de câncer cervical, é causado pela infecção persistente por alguns tipos do Papilomavírus Humano (HPV)1. É um dos mais frequentes tumores na população feminina e a quarta causa de morte de mulheres por câncer no Brasil2.
Entenda melhor o transplante de células-tronco
O Transplante de medula óssea é considerado um tratamento curativo para doenças onco-hematológicas e hematológicas que não respondem ao tratamento padrão (1, 2).
Panorama do diagnóstico de linfomas nos pacientes do SUS e mortalidade: análise de dados abertos
Introdução: O linfoma é um tipo de câncer que afeta os linfócitos, que são células responsáveis por proteger o corpo de infecções e doenças. O linfoma acontece quando os linfócitos e seus precursores que moram no sistema linfático, e que deveriam nos proteger contra as bactérias, vírus, dentre outros perigos, se transformam em malignos, crescendo de […]
Afinal, o que é o Programa Nacional de Apoio à Atenção Oncológica?

O Programa Nacional de Apoio à Atenção Oncológica (PRONON), instituído através da Lei nº 12.715 em 2012, foi desenvolvido para incentivar ações e serviços desenvolvidos por entidades, associações e fundações privadas sem fins lucrativos, que atuam no campo da oncologia na prevenção e combate ao câncer no Brasil (1).
Panorama do atendimento de pacientes diagnosticados com linfoma do manto no Brasil
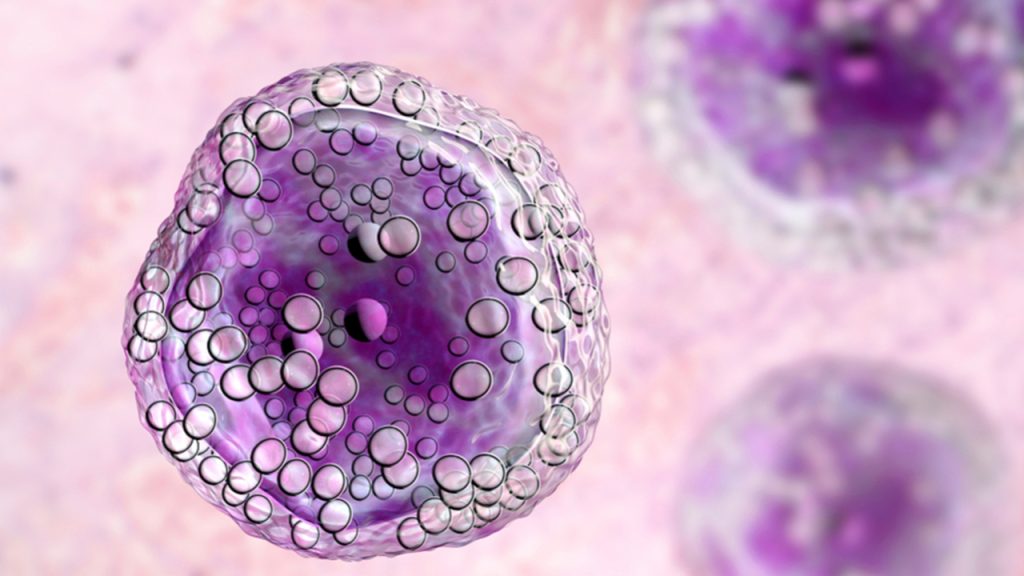
Linfomas são transformações neoplásicas de células linfoides normais que residem predominantemente em tecidos linfoides e são morfologicamente divididos em linfomas de Hodgkin (LH) e não-Hodgkin (LNH) (1). Os dois são distintos e se comportam de maneira bastante diferente, inclusive na resposta aos tratamentos (2). Segundo o Instituto Nacional de Câncer (INCA), para cada ano do […]
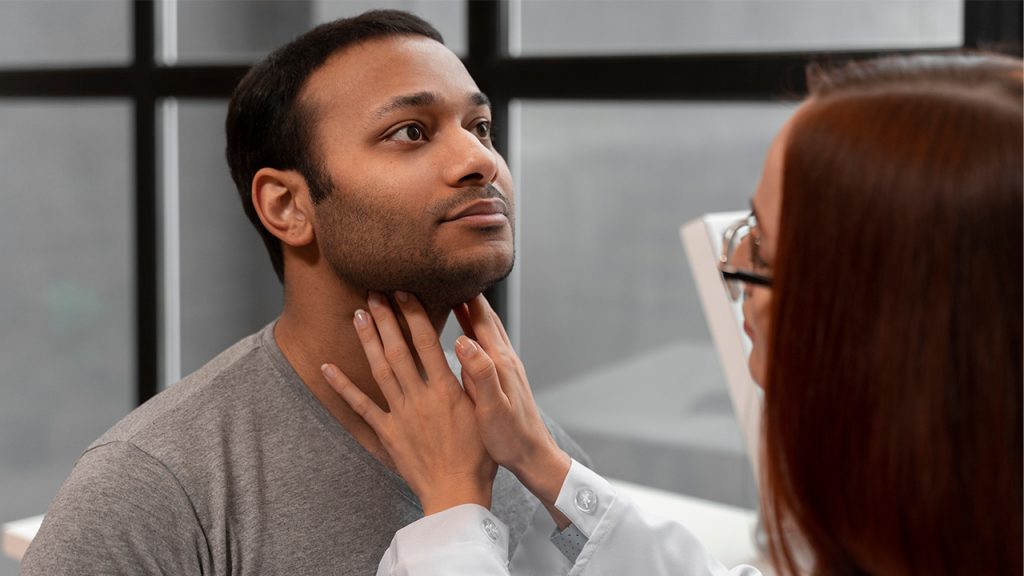
O melhor sorriso está guardado entre a cabeça e o pescoço
Epidemiologia Câncer de cabeça e pescoço é o nome genérico que se dá aos tumores que ocorrem na boca, na faringe, na laringe e nos seios paranasais. No Brasil não se tem uma incidência bem definida dos cânceres da cabeça e do pescoço. No mundo, em 2020, foram estimados 931.931 novos casos de câncer de […]
Atlas de Câncer de Pulmão
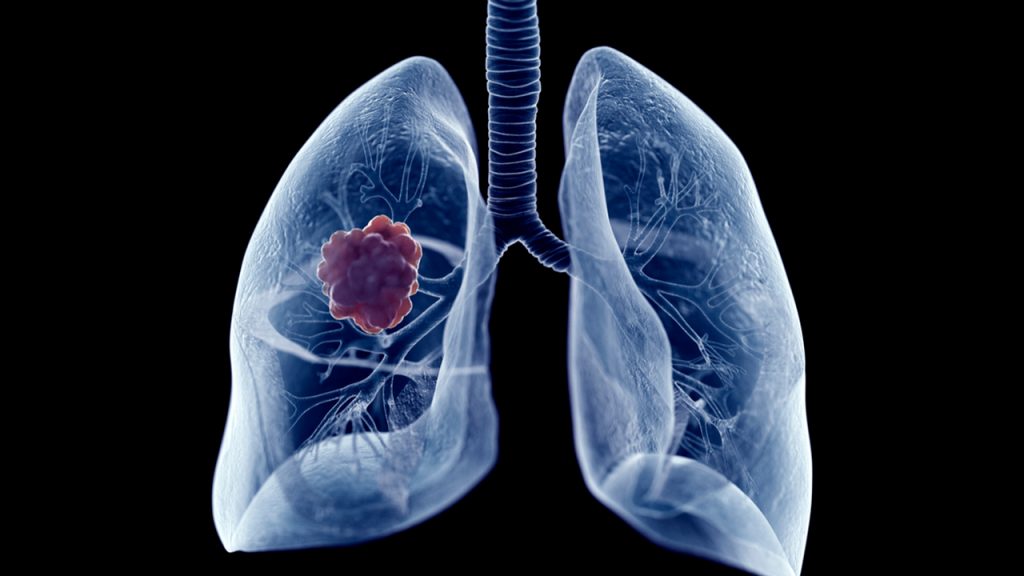
O câncer de pulmão é o segundo mais comum no mundo ocupando a primeira posição entre os homens e terceira posição entre as mulheres (IARC, 2020). No Brasil, é o quarto tipo mais incidente (sem contar o câncer de pele não melanoma), ocupando a terceira posição entre os homens e a quarta posição entre as […]
